Viri električnega toka
Električni tok - kako ga ustvariti in vzdrževati
 Urejeno gibanje nabitih delcev imenujemo električni tok. Če želite v žici dobiti električni tok, morate v njej ustvariti električno polje. Če naelektreno telo z žico povežemo z zemljo, se v žici pojavi kratkotrajni električni tok. Za pridobitev in vzdrževanje električnega polja v žici uporabite vire električnega toka.
Urejeno gibanje nabitih delcev imenujemo električni tok. Če želite v žici dobiti električni tok, morate v njej ustvariti električno polje. Če naelektreno telo z žico povežemo z zemljo, se v žici pojavi kratkotrajni električni tok. Za pridobitev in vzdrževanje električnega polja v žici uporabite vire električnega toka.
V vsakem viru toka poteka delo za ločevanje pozitivno in negativno nabitih delcev. Izločeni delci se kopičijo na polih vira. Med poloma se ustvari električno polje. Če jih povežete z žico, potem nastane polje v žici.
V električnem stroju se ločevanje nabojev izvede s pomočjo mehanske energije. Hkrati postane električna. V termočlenu se notranja energija pretvori v električno energijo. Jedrske baterije pretvarjajo atomsko energijo v elektriko.
Fotocelica pretvarja svetlobno energijo v električno. Sončne celice so sestavljene iz fotocelic.Uporabljajo se tam, kjer je svetlobna energija najbolj dostopna.
Energija rek, premoga, nafte in atomov se v elektrarnah pretvarja v električno energijo. Najpogostejši viri električnega toka so galvanski členi in baterije.
Galvanski členi
Galvanski člen je vir toka, v katerem se kemična energija pretvarja v električno.
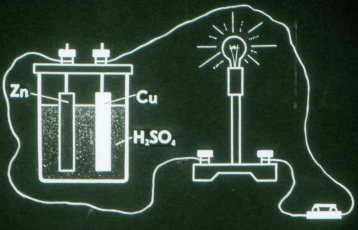
Tako deluje najpreprostejši galvanski člen.
Prvi elektrokemični člen je izumil Volt leta 1799. Iz posameznih elementov je sestavil baterijo, ki jo je poimenoval "voltov pol". V galvanskem členu morajo elektrode nujno komunicirati z raztopino na različne načine, zato so elektrode izdelane iz različnih materialov.

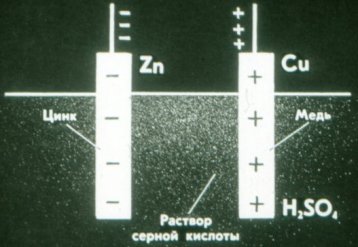
Cinkova plošča v Voltovi celici je negativno nabita, bakrena plošča pa pozitivno.
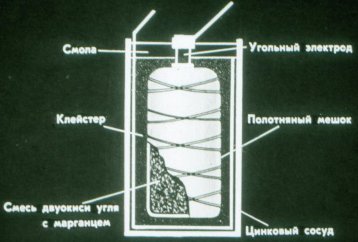
In tako deluje suhi galvanski člen. Namesto tekočine uporablja gosto pasto:
Baterija je lahko sestavljena iz več elementov:

Žarnice v električnih svetilkah, pa tudi raznih drugih prenosnih električnih napravah in otroških igračah se napajajo z galvanskimi členi. Ko so elektrode v galvanskem členu izrabljene, se člen zamenja z novim.
Baterije
Baterije so kemični viri električnega toka, pri katerih se elektrode ne porabljajo. Najpreprostejši akumulator je sestavljen iz dveh svinčenih plošč, potopljenih v raztopino žveplove kisline.
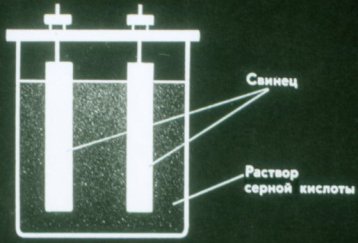
Takšna baterija še vedno ne daje toka. Pred uporabo ga je treba napolniti. Če želite to narediti, priključite pole baterije na iste pole vsakega vira toka.
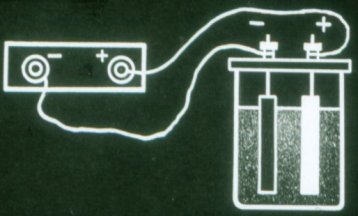
Tok, ki teče skozi baterijo med polnjenjem, spremeni kemično sestavo njenih plošč. Kemična energija baterije se poveča.
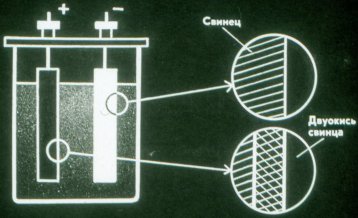
Ko se baterija izprazni, pretvori kemično energijo v električno. Izpraznjeno baterijo lahko ponovno napolnite.
Baterije se zbirajo iz ločenih baterij.
Poleg kislinskih (svinčevih) baterij se uporabljajo tudi alkalne (železo-nikelj) baterije.
Nikelj železova baterija:
Danes se pogosto uporabljajo tudi nikelj-kadmijeve in nikelj-metal-hidridne baterije. Srebrno-cinkove baterije se uporabljajo v letalstvu in vesolju, nove vrste baterij: litij-ionske, litij-polimerne pa se uporabljajo v mobilnih telefonih, tablicah in drugi sodobni prenosni opremi.
Baterije se uporabljajo v primerih, ko je vir električnega toka bolj donosno napolniti kot zamenjati z novim. V avtomobilu se akumulator uporablja za zagon motorja in delovanje različnih naprav. V vesolju baterijo polnijo sončne celice. Ko je izpraznjen, napaja radijske oddajnike in opremo.
Poglej tudi: Baterije. Primeri izračunov

